वह प्रक्रम जिसमें विद्युत ऊर्जा को रासायनिक ऊर्जा में परिवर्तित किया जाता है उसे विद्युत अपघटन कहते हैं।
विद्युत अपघटनी सेल
विद्युत अपघटनी प्रक्रमों में विद्युत ऊर्जा को रासायनिक ऊर्जा में परिवर्तित किया जाता है जिस युक्ति में विद्युत अपघटन की प्रक्रिया संपन्न की जाती है उसे विद्युत अपघटनी सेल (electrolytic cell in Hindi) कहते हैं।
विद्युत अपघटन की प्रक्रिया में बाह्य स्रोत से विद्युत ऊर्जा को एक विद्युत अपघट्य के विलयन में प्रवाहित किया जाता है।
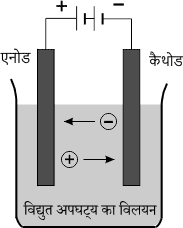
एक सामान्य विद्युत अपघटनी सेल को चित्र में प्रस्तुत किया गया है। विद्युत अपघटनी सेल का कैथोड बैटरी के ऋणात्मक ध्रुव से जुड़ा होता है तथा एनोड बैटरी के धनात्मक ध्रुव से जुड़ा होता है।
विद्युत अपघटनी सेल की क्रियाविधि
चित्र के अनुसार एक पात्र में विद्युत अपघट्य का विलयन है जिसमें दो इलेक्ट्रोड को एक बाह्य विद्युत स्रोत बैटरी से जोड़ा गया है। बैटरी के धन टर्मिनल से जुड़े इलेक्ट्रोड को एनोड कहते हैं तथा बैटरी के ऋण टर्मिनल से जुड़े इलेक्ट्रोड को कैथोड कहते हैं। धनायन, कैथोड की ओर गति कर कैथोड पर अपचयित होते हैं तथा ऋणायन, एनोड की ओर गति कर एनोड पर ऑक्सीकृत हो जाते हैं।
गलित सोडियम क्लोराइड का विद्युत अपघटन :- विद्युत धारा प्रवाहित करने पर Na+ आयन कैथोड की ओर तथा Cl– आयन एनोड की ओर गति करते हैं। प्रत्येक Na+ आयन कैथोड से एक इलेक्ट्रॉन ग्रहण कर Na परमाणु में अपचयित होता है। जबकि प्रत्येक Cl+ आयन एनोड को एक इलेक्ट्रॉन त्याग कर Cl परमाणु में ऑक्सीकृत हो जाता है।
इनकी अभिक्रिया निम्न प्रकार से हैं।
कैथोड पर Na+ + e– → Na (अपचयन)
एनोट पर Cl– – e– → Cl (ऑक्सीकरण)
विद्युत अपघटन के अन्य उदाहरण
- प्लैटिनम इलेक्ट्रोडों का प्रयोग कर जलीय कॉपर सल्फेट विलयन का विद्युत अपघटन
- कॉपर इलेक्ट्रोडों का प्रयोग कर जलीय कॉपर सल्फेट विलयन का विद्युत अपघटन

